


БНБ
"БСЭ" (95279)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Стронций
Определение "Стронций" в Большой Советской Энциклопедии
Стронций (лат. Strontium), Sr, химический элемент II группы периодической Системы Менделеева, атомный номер 38, атомная масса 87,62, серебристо-белый металл. Природный Стронций состоит из смеси четырёх стабильных изотопов: 84Sr, 86Sr, 87Sr и 88Sr; наиболее распространён 88Sr (82,56%).
Искусственно получены радиоактивные изотопы с массовыми числами от 80 до 97, в том числе 90Sr (Т 1/2 = 27,7 года), образующийся при делении урана. В 1790 шотландский врач А. Крофорд, исследуя найденный близ населённого пункта Строншиан (в Шотландии) минерал, обнаружил, что он содержит неизвестную ранее «землю», которая была названа стронцианом. Позднее оказалось, что это окись Стронций SrO. В 1808 Г. Дэви, подвергая электролизу с ртутным катодом смесь увлажнённой гидроокиси Sr(ОН)2 с окисью ртути, получил амальгаму Стронций
Распространение в природе. Среднее содержание Стронций в земной коре (кларк) 3,4-102% по массе, в геохимических процессах он является спутником кальция. Известно около 30 минералов Стронций: важнейшие — целестин SrSO4 и стронцианит SrCO3. В магматических породах Стронций находится преимущественно в рассеянном виде и входит в виде изоморфной примеси в кристаллическую решётку кальциевых, калиевых и бариевых минералов. В биосфере Стронций накапливается в карбонатных породах и особенно в осадках солёных озёр и лагун (месторождения целестина).
Физические и химические свойства. При комнатной температуре решётка Стронций кубическая гранецентрированная (a-Sr) с периодом а = 6,0848 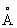 ; при температуре выше 248 °С превращается в гексагональную модификацию (b-Sr) с периодами решётки а=4,32
; при температуре выше 248 °С превращается в гексагональную модификацию (b-Sr) с периодами решётки а=4,32 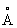 и с = 7,06
и с = 7,06 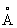 ; при 614 °С переходит в кубическую объёмноцентрированную модификацию (g-Sr) с периодом а = 4,85
; при 614 °С переходит в кубическую объёмноцентрированную модификацию (g-Sr) с периодом а = 4,85 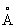 . Атомный радиус 2,15
. Атомный радиус 2,15 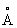 , ионный радиус Sr2 + 1,20
, ионный радиус Sr2 + 1,20 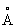 . Плотность a - формы 2,63г/см3 (20 °С); tпл 770 °С, tkип 1383 °С; удельная теплоёмкость 737,4 кдж/(кг·К) [0,176 кал/(г·°С)]; удельное электросопротивление 22.76-10-6ом·см3 Стронций парамагнитен, атомная магнитная восприимчивость при комнатной температуре 91,2·10-6. Стронций — мягкий пластичный металл, легко режется ножом. Конфигурация внешней электронной оболочки атома Sr 5s2, в соединениях обычно имеет степень окисления +2. Стронций — щёлочноземельный металл, по химическим свойствам сходен с Ca и Ba. Металлический Стронций быстро окисляется на воздухе, образуя желтоватую поверхностную плёнку, содержащую окись SrO, перекись SrO2 и нитрид Sr3N2. С кислородом при обычных условиях образует окись SrO (серовато-белый порошок), которая на воздухе легко переходит в карбонат SrCO3: с водой энергично взаимодействует, образуя гидроокись Sr (OH)2 — основание более сильное, чем Ca (OH)2. При нагревании на воздухе легко воспламеняется, а порошкообразный Стронций на воздухе самовозгорается, поэтому хранят Стронций в герметически закрытых сосудах под слоем керосина. Бурно разлагает воду с выделением водорода и образованием гидроокиси. При повышенных температурах взаимодействует с водородом (>200 °С), азотом (>400 °С), фосфором, серой и галогенами. При нагревании образует интерметаллические соединения с металлами, например SrPb3, SrAg4, SrHg8, SrHg12. Из солей Стронций хорошо растворимы в воде галогениды (кроме фторида), нитрат, ацетат, хлорат; трудно растворимы карбонат, сульфат, оксалат и фосфат. Осаждение Стронций в виде оксалата и сульфата используют для его аналитического определения. Многие соли Стронций образуют кристаллогидраты, содержащие от 1 до 6 молекул кристаллизационной воды. Сульфид SrS постепенно гидролизуется водой: нитрид Sr3N2 (чёрные кристаллы) легко разлагается водой с выделением NH3 и Sr (OH)2. Стронций хорошо растворяется в жидком аммиаке, давая растворы тёмно-синего цвета.
. Плотность a - формы 2,63г/см3 (20 °С); tпл 770 °С, tkип 1383 °С; удельная теплоёмкость 737,4 кдж/(кг·К) [0,176 кал/(г·°С)]; удельное электросопротивление 22.76-10-6ом·см3 Стронций парамагнитен, атомная магнитная восприимчивость при комнатной температуре 91,2·10-6. Стронций — мягкий пластичный металл, легко режется ножом. Конфигурация внешней электронной оболочки атома Sr 5s2, в соединениях обычно имеет степень окисления +2. Стронций — щёлочноземельный металл, по химическим свойствам сходен с Ca и Ba. Металлический Стронций быстро окисляется на воздухе, образуя желтоватую поверхностную плёнку, содержащую окись SrO, перекись SrO2 и нитрид Sr3N2. С кислородом при обычных условиях образует окись SrO (серовато-белый порошок), которая на воздухе легко переходит в карбонат SrCO3: с водой энергично взаимодействует, образуя гидроокись Sr (OH)2 — основание более сильное, чем Ca (OH)2. При нагревании на воздухе легко воспламеняется, а порошкообразный Стронций на воздухе самовозгорается, поэтому хранят Стронций в герметически закрытых сосудах под слоем керосина. Бурно разлагает воду с выделением водорода и образованием гидроокиси. При повышенных температурах взаимодействует с водородом (>200 °С), азотом (>400 °С), фосфором, серой и галогенами. При нагревании образует интерметаллические соединения с металлами, например SrPb3, SrAg4, SrHg8, SrHg12. Из солей Стронций хорошо растворимы в воде галогениды (кроме фторида), нитрат, ацетат, хлорат; трудно растворимы карбонат, сульфат, оксалат и фосфат. Осаждение Стронций в виде оксалата и сульфата используют для его аналитического определения. Многие соли Стронций образуют кристаллогидраты, содержащие от 1 до 6 молекул кристаллизационной воды. Сульфид SrS постепенно гидролизуется водой: нитрид Sr3N2 (чёрные кристаллы) легко разлагается водой с выделением NH3 и Sr (OH)2. Стронций хорошо растворяется в жидком аммиаке, давая растворы тёмно-синего цвета.
Получение и применение. Основным сырьём для получения соединений Стронций служат концентраты от обогащения целестина и стронцианита. Металлический Стронций получают восстановлением окиси Стронций алюминием при 1100—1150 °С:
Процесс ведут в электровакуумных аппаратах [при 1 н/м2 (10 -2 мм рт. ст.)] периодического действия. Пары Стронций конденсируются на охлажденной поверхности вставленного в аппарат конденсатора; по окончании восстановления аппарат заполняют аргоном и расплавляют конденсат, который стекает в изложницу. Стронций получают также электролизом расплава, содержащего 85% SrCl2 и 15% KCI, однако при этом процессе выход по току невелик, а металл оказывается загрязнённым солями, нитридом и окисью. В промышленности электролизом с жидким катодом получают сплавы Стронций, например с оловом.
Практическое применение металлического Стронций невелико. Он служит для раскисления меди и бронзы. -90Sr — источник b-излучения в атомных электрических батареях. Стронций используется для изготовления люминофоров и фотоэлементов, а также сильно пирофорных сплавов. Окись Стронций входит в состав некоторых оптических стекол и оксидных катодов электронных ламп. Соединения Стронций окрашивают пламя в интенсивный вишнёво-красный цвет, благодаря чему некоторые из них находят применение в пиротехнике. Стронцианит вводят в шлак для очистки высокосортных сталей от серы и фосфора; карбонат Стронций используют в неиспаряющихся геттерах, а также добавляют в состав стойких к атмосферным воздействиям глазурей и эмалей для покрытия фарфора, сталей и жаропрочных сплавов. Хромат SrCrO4 — очень устойчивый пигмент для изготовления художественных красок, титанат SrTiO3 применяют как сегнетоэлектрик, он входит в состав пьезокерамики. Стронциевые соли жирных кислот («стронциевые мыла») используют для изготовления специальных консистентных смазок.
Соли и соединения Стронций малотоксичны; при работе с ними следует руководствоваться правилами техники безопасности с солями щелочных и щёлочноземельных металлов. См. также разделы Стронций в организме и Стронций-90.
М. Е. Ерлыкина.
Стронций в организме. Стронций — составная часть микроорганизмов, растений и животных. У морских радиолярий (акантарий) скелет состоит из сульфата Стронций — целестина. Морские водоросли содержат 26—140 мг Стронций на 100 г сухого вещества, наземные растения — 2,6, морские животные — 2—50, наземные животные — 1,4, бактерии — 0,27—30. Накопление Стронций различными организмами зависит не только от их вида, особенностей, но и от соотношения в среде Стронций с др. элементами, главным образом с Ca и Р, а также от адаптации организмов к определённой геохимической среде.
Животные получают Стронций с водой и пищей. Всасывается Стронций тонким, а выделяется в основном толстым кишечником. Ряд веществ (полисахариды водорослей, катионообменные смолы) препятствует усвоению Стронций Главное депо Стронций в организме — костная ткань, в золе которой содержится около 0,02% Стронций (в др. тканях — около 0,0005%). Избыток солей Стронций в рационе крыс вызывает «стронциевый» рахит. У животных, обитающих на почвах со значительным количеством целестина, наблюдается повышенное содержание Стронций в организме, что приводит к ломкости костей, рахиту и др. заболеваниям. В биогеохимических провинциях, богатых Стронций (ряд районов Центральной и Восточной Азии, Северной Европы и др.), возможна т. н. уровская болезнь.
Г. Г. Поликарпов.
Стронций-90. Среди искусственных изотопов Стронций его долгоживущий радионуклид 90Sr — один из важных компонентов радиоактивного загрязнения биосферы. Попадая в окружающую среду, 90Sr характеризуется способностью включаться (главным образом вместе с Ca) в процессы обмена веществ у растений, животных и человека. Поэтому при оценке загрязнения биосферы 90Sr принято рассчитывать отношение 90Sr/Ca в стронциевых единицах (1 с. е. = 1 мк мккюри 90Sr на 1 г Ca). При передвижении 90Sr и Ca по биологическим и пищевым цепям происходит дискриминация Стронций, для количественного выражения которой находят «коэффициент дискриминации», отношение 90Sr/Ca в последующем звене биологической или пищевой цепи к этой же величине в предыдущем звене. В конечном звене пищевой цепи концентрация 90Sr, как правило, значительно меньше, чем в начальном.
В растения 90Sr может поступать непосредственно при прямом загрязнении листьев или из почвы через корни (при этом большое влияние имеет тип почвы, сё влажность, pH, содержание Ca и органических веществ и т.д.). Относительно больше накапливают 90Sr бобовые растения, корне- и клубнеплоды, меньше — злаки, в том числе зерновые, и лён. В семенах и плодах накапливается значительно меньше 90Sr, чем в др. органах (например, в листьях и стеблях пшеницы 90Sr в 10 раз больше, чем в зерне). У животных (поступает в основном с растительной пищей) и человека (поступает в основном с коровьим молоком и рыбой) 90Sr накапливается главным образом в костях. Величина отложения 90Sr в организме животных и человека зависит от возраста особи, количества поступающего радионуклида, интенсивности роста новой костной ткани и др. Большую опасность 90Sr представляет для детей, в организм которых он поступает с молоком и накапливается в быстро растущей костной ткани.
Биологическое действие 90Sr связано с характером его распределения в организме (накопление в скелете) и зависит от дозы b-облучения, создаваемого им и его дочерним радиоизотопом 90Y. При длительном поступлении 90Sr в организм даже в относительно небольших количествах, в результате непрерывного облучения костной ткани, могут развиваться лейкемия и рак костей. Существенные изменения в костной ткани наблюдаются при содержании "°Sr в рационе около 1 мккюри на 1 г Ca. Заключение в 1963 в Москве Договора о запрещении испытаний ядерного оружия в атмосфере, космосе и под водой привело к почти полному освобождению атмосферы от 90Sr и уменьшению его подвижных форм в почве.
В. А. Кальченко.
Лит.: Бурков В. В., Подпоряна Е. К., Стронций, М., 1962; Булдаков Л. А. и Москалев Ю. И., Проблемы распределения и экспериментальной оценки допустимых уровней Cs137, Sr90 и Ru106, М., 1968; Юдинцева Е. В., Гулякин И. В., Агрохимия радиоактивных изотопов стронция и цезия, М., 1968; Метаболизм стронция. Сб. статей, пер. с англ., М., 1971; Радиоактивность и пища человека, пер. с англ., М., 1971; Ковальский В. В., Геохимическая экология, М., 1974; Хеморадиоэкология пелагиали и бентали, К., 1974; Bowen Н. J. М., Trace elemetns in biochemistry, L. — N. Y., 1966.
| "БСЭ" >> "С" >> "СТ" >> "СТР" >> "СТРО" |
Статья про "Стронций" в Большой Советской Энциклопедии была прочитана 515 раз
| Пицца в сковороде |
| Сингапурский салат |
TOP 20
- Лемке Михаил Константинович
- Сульфгидрильные группы
- «Казарменный коммунизм»
- Глициния
- Японское море
- Периодическая система элементов
- Башкирская Автономная Советская Социалистическая Республика
- Иммунитет (историч.)
- Андаманское море
- Сенсуализм
- «Сообразительный»
- Звёздная астрономия
- Балкано-кавказская раса
- Ямполь (пос. гор. типа в Донецкой обл.)
- Навигация (морск.)
- Кульчицкая Елена Львовна
- Мандельштама - Бриллюэна рассеяние
- Театральные учебные заведения
- Электрическая постоянная
- Энсор Джеймс