


БНБ
"БСЭ" (95279)
- Photogallery
- Естественные науки - Математика - Технология
- Авиация и машиностроение
- Высокие технологии
- Вычислительная техника
- Нанотехнология
- Роботехника
- Энергетика
- Электроника
Уравнение состояния
Определение "Уравнение состояния" в Большой Советской Энциклопедии
Уравнение состояния, связывает давление р, объём V и температуру Т физически однородной системы в состоянии равновесия термодинамического: f (p, V, Т) = 0. Это уравнение называется термическим Уравнение состояния, в отличие от калорического Уравнение состояния, определяющего внутреннюю энергию системы U как функцию какого-либо двух из трёх параметров р, V, Т. Термическое Уравнение состояния позволяет выразить давление через объём и температуру р = p (V, Т) и определить элементарную работу dA = = pdV при бесконечно малом расширении системы dV. Уравнение состояния является необходимым дополнением к термодинамическим законам, которое делает возможным их применение к реальным веществам. Оно не может быть выведено с помощью одних только законов термодинамики, а определяется или рассчитывается теоретически на основе представлений о строении вещества методами статистической физики. Из первого начала термодинамики следует лишь существование калорического Уравнение состояния, а из второго начала термодинамики – связь между термическим и калорическим Уравнение состояния 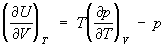 , откуда вытекает, что для идеального газа внутренняя энергия не зависит от объёма
, откуда вытекает, что для идеального газа внутренняя энергия не зависит от объёма 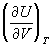 = 0. Термодинамика показывает, что для вычисления как термического, так и калорического Уравнение состояния, достаточно знать любой из потенциалов термодинамических в виде функции своих параметров. Например, если известна Гельмгольцева энергия F как функция Т и V, то Уравнение состояния находят дифференцированием:
= 0. Термодинамика показывает, что для вычисления как термического, так и калорического Уравнение состояния, достаточно знать любой из потенциалов термодинамических в виде функции своих параметров. Например, если известна Гельмгольцева энергия F как функция Т и V, то Уравнение состояния находят дифференцированием: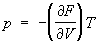 ,
, 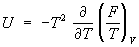 .
.
Примерами Уравнение состояния для газов может служить Клапейрона уравнение для идеального газа pu = RT, где R – газовая постоянная, u – объём 1 моля газа;
Ван-дер-Ваальса уравнение 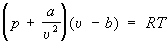 , где а и b – постоянные, зависящие от природы газа и учитывающие влияние сил притяжения между молекулами и конечность из объёма, вириальное Уравнение состояния для неидеального pu / RT = 1 + B (T)/ u + С (Т)/ u2 +.., где В (Т), С (Т)... – 2-й, 3-й и т.д. вириальные коэффициенты, зависящие от сил взаимодействия между молекулами (см. Газы). Это уравнение является наиболее надёжным и теоретически обоснованным Уравнение состояния для газов и позволяет объяснить многочисленные экспериментальные результаты на основании простых моделей межмолекулярного взаимодействия. Были предложены также различные эмпирические Уравнение состояния, основанные на экспериментальных данных о теплоёмкости и сжимаемости. Уравнение состояния неидеальных газов указывает на существование критической точки (с параметрами pk, Vk, Tk), в которой газообразная и жидкая фазы становятся идентичными (см. Критическое состояние). Если Уравнение состояния представить в виде приведенного Уравнение состояния, т. е. в безразмерных переменных p/pk, V/Vk, T/Tk, то при не слишком низких температурах это уравнение мало меняется для различных веществ (закон соответственных состояний).
, где а и b – постоянные, зависящие от природы газа и учитывающие влияние сил притяжения между молекулами и конечность из объёма, вириальное Уравнение состояния для неидеального pu / RT = 1 + B (T)/ u + С (Т)/ u2 +.., где В (Т), С (Т)... – 2-й, 3-й и т.д. вириальные коэффициенты, зависящие от сил взаимодействия между молекулами (см. Газы). Это уравнение является наиболее надёжным и теоретически обоснованным Уравнение состояния для газов и позволяет объяснить многочисленные экспериментальные результаты на основании простых моделей межмолекулярного взаимодействия. Были предложены также различные эмпирические Уравнение состояния, основанные на экспериментальных данных о теплоёмкости и сжимаемости. Уравнение состояния неидеальных газов указывает на существование критической точки (с параметрами pk, Vk, Tk), в которой газообразная и жидкая фазы становятся идентичными (см. Критическое состояние). Если Уравнение состояния представить в виде приведенного Уравнение состояния, т. е. в безразмерных переменных p/pk, V/Vk, T/Tk, то при не слишком низких температурах это уравнение мало меняется для различных веществ (закон соответственных состояний).
Для равновесного излучения, или фотонного газа, Уравнение состояния определяется Планка законом излучения для средней плотности энергии.
Для жидкостей из-за сложности учёта всех особенностей взаимодействия молекул пока не удалось теоретически получить общее Уравнение состояния Уравнение Ван-дер-Ваальса хотя и применяют для качественной оценки поведения жидкостей, но оно по существу неприменимо ниже критической точки, когда возможно сосуществование жидкой и газообразной фаз. Уравнение состояния, хорошо описывающее свойства ряда простых жидкостей, можно получить из приближённых теорий жидкого состояния типа теории свободного объёма или дырочной теории (см. Жидкость). Знание распределения вероятности взаимного расположения молекул (парной корреляционной функции) принципиально позволяет вычислить Уравнение состояния жидкости, но эта задача очень сложна и полностью ещё не решена даже с помощью вычислительных машин.
Для твёрдых тел термическое Уравнение состояния определяет зависимость модулей упругости от температуры и давления. Оно может быть получено на основании теории теплового движения в кристаллах, рассматривающей фононы и их взаимодействие, но пока общего Уравнение состояния для твёрдых тел не найдено.
Для магнитных сред элементарная работа при намагничивании равна dA = -НdМ, где М – магнитный момент, Н – напряжённость магнитного поля. Следовательно, зависимость М = М (Н, Т) представляет собой магнитное Уравнение состояния
Для электрически поляризуемых сред элементарная работа при поляризации равна dA = -ЕdР где Р - поляризация, Е - напряжённость электрического поля, следовательно, Уравнение состояния имеет вид Р = (Е, Т).
Лит.: Хилл Т., Статистическая механика, пер. с англ., М., 1960; Вукалович М. П., Новиков И. И., Уравнение состояния реальных газов, М. – Л., 1948; Мейсон Э., Сперлинг Т., Вириальное уравнение состояния, пер. с англ., М., 1972; Лейбфрид Г., Людвиг В., Теория ангармонических эффектов в кристаллах, пер. с англ., М., 1963. См. также лит. при статьях Статистическая физика и Термодинамика.
Д. Н. Зубарев.
| "БСЭ" >> "У" >> "УР" >> "УРА" |
Статья про "Уравнение состояния" в Большой Советской Энциклопедии была прочитана 827 раз
| Бургер двойного помола |
| Панайпай |
TOP 20
- Лемке Михаил Константинович
- Сульфгидрильные группы
- «Казарменный коммунизм»
- Глициния
- Японское море
- Периодическая система элементов
- Башкирская Автономная Советская Социалистическая Республика
- Иммунитет (историч.)
- Андаманское море
- Сенсуализм
- «Сообразительный»
- Звёздная астрономия
- Балкано-кавказская раса
- Ямполь (пос. гор. типа в Донецкой обл.)
- Навигация (морск.)
- Кульчицкая Елена Львовна
- Мандельштама - Бриллюэна рассеяние
- Театральные учебные заведения
- Электрическая постоянная
- Энсор Джеймс